● 医薬品情報室-79
経鼻弱毒生インフルエンザワクチン(フルミスト点鼻液)
2025.2.1
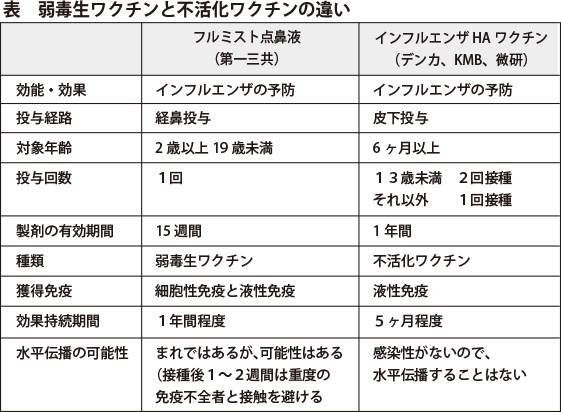
2024 年 10 月、国内初の経鼻(鼻腔噴霧型)インフルエンザワクチン、フルミスト点鼻液(一般名:経鼻弱毒生インフルエンザワクチン)が発売されました。接種対象者は2歳以上19歳未満で、既存の不活化インフルエンザHAワクチンに比べ、「注射せず痛くない」「1回の接種で済む」などのメリットがあります。
インフルエンザは、健康な人ではシビアな全身症状があったとしても、命に別状はありません。しかし乳幼児や高齢者が罹患すると、急性脳症(乳幼児)や続発性細菌性肺炎(高齢者)などの重度合併症を引き起こすことがあります。インフルエンザに関連する超過死亡数は、年間1万人を超えると推定されています。
臨床的に問題となるインフルエンザウイルスは、A型とB型株です。1つの宿主細胞に複数のウイルスが重複感染すると、遺伝子の一部が入れ替わるリアソータント(遺伝子再集合)という現象が起こります。フルミスト点鼻液は、A型2種とB型2種の4価のリアソータントウイルス株からなります。低温(25度)で効率よく増殖する株を継代培養して弱毒ウイルスを作成します(低温馴化)。B型株は37度、A型株は39度で増殖しにくくなります(温度感受性)。感染モデルのフェレットを発症させません(弱毒化)。鼻腔内に噴霧すると、上部気道(33度)の上皮細胞で増殖して獲得免疫を誘導しますが、肺などの下部気道(37度)では活性が著しく低下します。生ワクチンなので、細胞性免疫(T細胞による直接攻撃)と液性免疫(B細胞による抗体産生)の両方を誘導します。重症化予防効果がある血中IgG抗体だけでなく、皮下注では誘導できない粘膜上の分泌型IgA抗体も産生し、鼻粘膜や咽喉からのウイルス侵入を防ぐ発症予防効果が期待されます。不活化インフルエンザHAワクチンとほぼ同等の効果が認められました。海外では、2003年に米国で承認され、適応年齢が米国49歳以下、EU17歳以下と日本とは異なります。高齢者は免疫応答が弱いため適応対象外となります。そのほか製剤の有効期限が15週間と短いこと、皮下接種ワクチンには公費補助があるが経鼻噴霧ワクチンにはない自治体があるなどのデメリットがあります。
日本小児科学会は『経鼻弱毒生インフルエンザワクチンの使用に関する考え方』を公表し、2〜19歳未満に対しては、不活化インフルエンザHAワクチンと経鼻弱毒生インフルエンザワクチンを同等に推奨する。喘息患者、授乳婦、周囲に免疫不全患者がいる場合は不活化インフルエンザHAワクチンを推奨する。これは被接種者から未接種者への水平伝播のリスクが懸念されるためです(いわゆるシェディング)。また、生後6ヵ月〜2歳未満、19歳以上、免疫不全患者、無脾症患者、妊婦、ミトコンドリア脳筋症患者、ゼラチンアレルギーを有する患者、中枢神経系の解剖学的バリアー破綻がある患者に対しては、不活化インフルエンザHAワクチンのみを推奨するとしています。