● 医薬品情報室-90
iPS細胞由来の再生医療等製品2製品が承認
2026.5.1
2026年3月、パーキンソン病治療用のアムシェプリ(一般名:ラグネプロセル)と重症心不全治療用のリハート〔構成細胞:ヒト(同種)iPS細胞由来心筋細胞シート〕が承認(条件及び期限付)されました。iPS細胞を用いた世界初となる再生医療等製品です。
iPS細胞(induced pluripotent stem cell)は、人工的に誘導した(インデュースト)、あらゆる細胞に分化できる多能性(プルリポテント)、幹細胞(ステム・セル)の略。皮膚や神経などに「分化した細胞」の時間を、受精卵のような「未分化な状態」に巻き戻した細胞です。2006年、京都大学の山中伸弥教授らはマウスの皮膚細胞(線維芽細胞)に、わずか4つの転写因子を導入することで、成熟細胞の初期化(リプログラミング)に成功。2012年にノーベル生理学・医学賞を受賞しました。受精卵から作製したES細胞(エンブリオニック・ステム・セル)のような倫理的な問題はありません。それから20年、ついに社会実装の段階になりました。アムシェプリは、健康なヒト(非自己)由来のiPS細胞を、ドパミン神経細胞に分化する手前のドパミン神経前駆細胞に誘導し、患者の脳内(線条体)に移植します。細胞が定着しドパミン産生が持続することで、運動症状を改善します。レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないパーキンソン病患者が対象です。リハートは、健康なヒト(同種)iPS細胞から作製した心筋細胞を、薄いシート状に加工して心臓表面に貼付します。移植後は、心筋として収縮するのではなく、細胞から分泌されるサイトカインなどの生理活性物質が心筋の修復を促します【パラクライン(傍分泌)効果】。既存の薬物療法や補助人工心臓などで効果が不十分な重症心不全患者が対象です。
再生医療(細胞治療)では、自家は患者自身(自己)、他家は他人(非自己)、同種はヒト同士、異種はブタなど、ヒト以外。他家(同種)末梢血由来は、健康な細胞提供者(ドナー)から採取した血液に由来するという意味。他家の場合、拒絶反応を防ぐため免疫抑制薬(タクロリムスなど)の投与が必要になります。
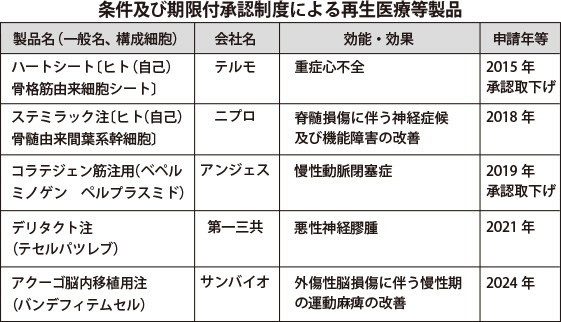
2014年の薬機法改正で、医薬品や医療機器のほかに、再生医療等製品が定義されました。医薬品は、第3相試験(対照薬と比較する、数千人規模の検証的試験)を経て承認されます。再生医療等製品は、個人差のある均質でない細胞や遺伝子を用いるため治験者数の確保が困難です。そこで、治療法のない患者にできるだけ早期に提供できる仕組みとして、有効性が「推定」され、安全性が「確認」された段階で「(仮)承認」し、使用を専門的な医師や設備がある医療機関に限定し、7年以内に再申請して「正式承認」を取得する『条件及び期限付承認制度』が導入されました。今回の承認も、対照なしの単群試験(7〜8例)。しかし、この日本独自の早期承認制度をもってしても、重症心不全のハートシートと閉塞性動脈硬化症のコラテジェンは有効性を検証できず撤退しました。リハートとハートシートの違いは、自分の骨格筋芽細胞か、他者のiPS細胞かだけ。海外では、開胸手術が必要なリハートに比べ、さらに低侵襲性のカテーテル投与製品が開発中。承認に必要な目標症例数は、アムシェプリが35例、リハートが75例。なお、両製品とも、1千万円を超えると推定される高額薬価のため、未だ保険適用の目途は立っていません。